计算化学和人工智能课题组近日在国际著名期刊Biomacromolecules、Colloids and Surfaces B: Biointerfaces上发表研究论文。该文章学生第一作者分别来自重庆三峡学院2025级硕士研究生赖睿鹏、聂余湘,通讯作者为宋先雨副教授。研究工作得到了广西大学赵双良教授、华东理工大学刘洪来教授的指导。
聚合物纳米颗粒在药物递送领域展现出独特优势,其不仅能包载多样化药物分子,还可通过表面工程设计实现靶向递送。然而,该技术的临床应用面临关键瓶颈:系统给药后仅约0.7%的纳米颗粒能抵达目标部位,且纳米颗粒刚度对细胞摄取的影响机制存在广泛争议。为解析这一难题,本研究通过大规模计算模拟与实验验证相结合的策略,系统揭示了结构异质性与力学性能的协同作用机制。研究发现,均质纳米颗粒主要通过膜破裂途径内化,而具有核壳或Janus结构的异质纳米颗粒则倾向于引发膜包裹,其穿透效率提升至均质颗粒的1.7-2.3倍。更重要的是,研究发现了结构变形与膜包裹之间的平衡关系:虽然变形会阻碍内化,但通过精准设计内部异质性可有效诱导膜包裹,从而克服这一限制。
随着生物膜和弹性聚合物纳米颗粒的内在结构变形,它们的相互作用最终形成了一个“软性”纳米-生物界面,该界面在生理上起到作为生物屏障的作用,从而阻止弹性纳米颗粒的穿透,如图1A所示。具体而言,在膜平面的横向方向上,存在自适应的机械和形态变形。对此,课题组建立了一个分子热力学-动力学(MTD)框架,该框架整合了粗粒化分子动力学、伞形采样、良好调控的元动力学和过渡态理论,以阐明弹性调控的渗透,如图1B所示。
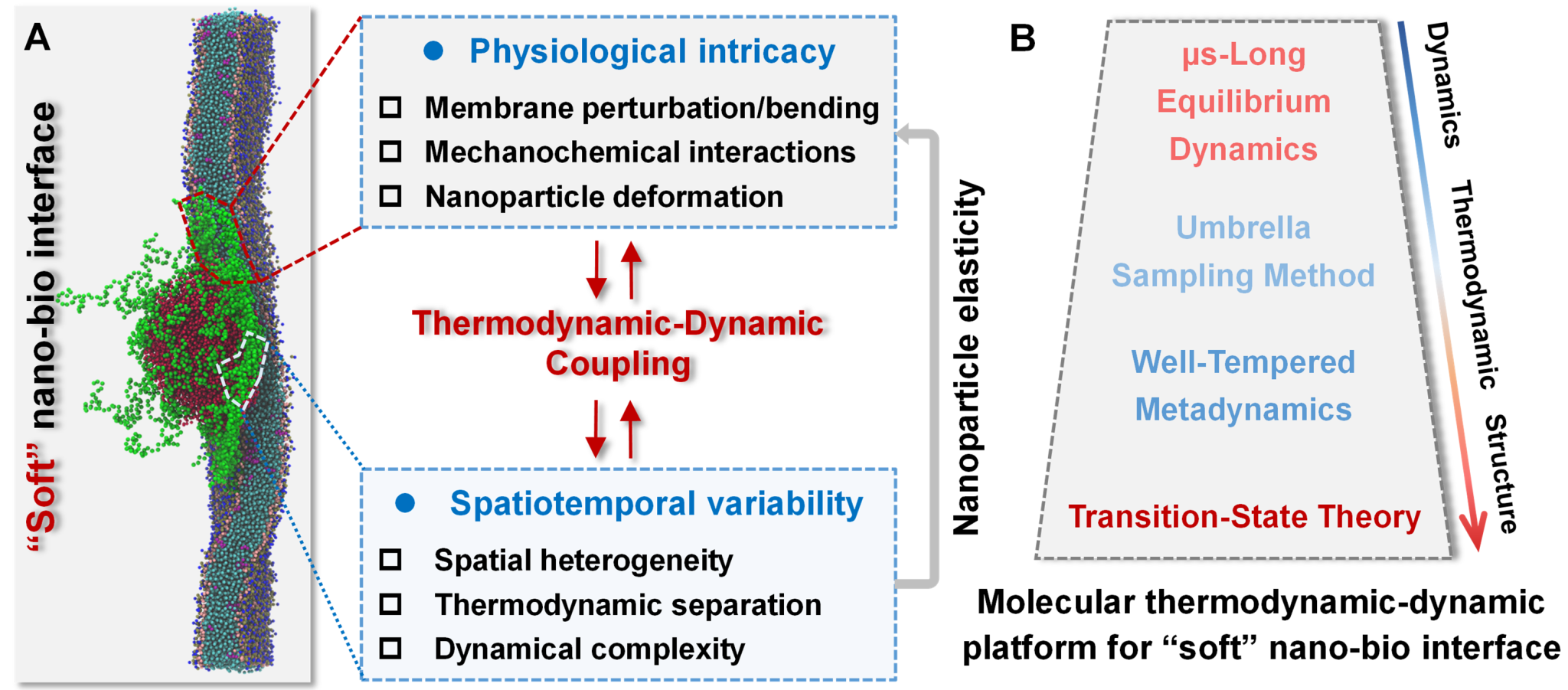
图1. (A)“软”纳米-生物界面的生物屏障示意图,具有时空异质性的特殊性质,(B)分子热力学-动力学(MTD)平台,考虑了微秒级的长期平衡动力学、伞式采样方法、良好调节的元动力学以及过渡态理论。对于快照(图1A),绿色表示亲水区,红色表示核壳纳米粒子的疏水区,溶剂和盐被省略以便清晰展示“软”纳米-生物界面。
图2揭示了纳米颗粒(NP)刚度对其细胞膜穿透动力学与膜结构响应的调控机制。研究表明,硬质NPs(~5.2 MPa)表现出快速、持续的膜吞噬和垂直的直接穿透路径;软质NPs(~68.9 kPa)则呈现缓慢、渐进的膜包覆与横向扩散,多停留于表面锚定状态;而中等刚度NPs(~127.3 kPa)展现出介于二者之间的过渡行为。此连续变化规律表明,NPs的机械特性是调控其内吞模式与膜作用动力学的关键物理决定因素。
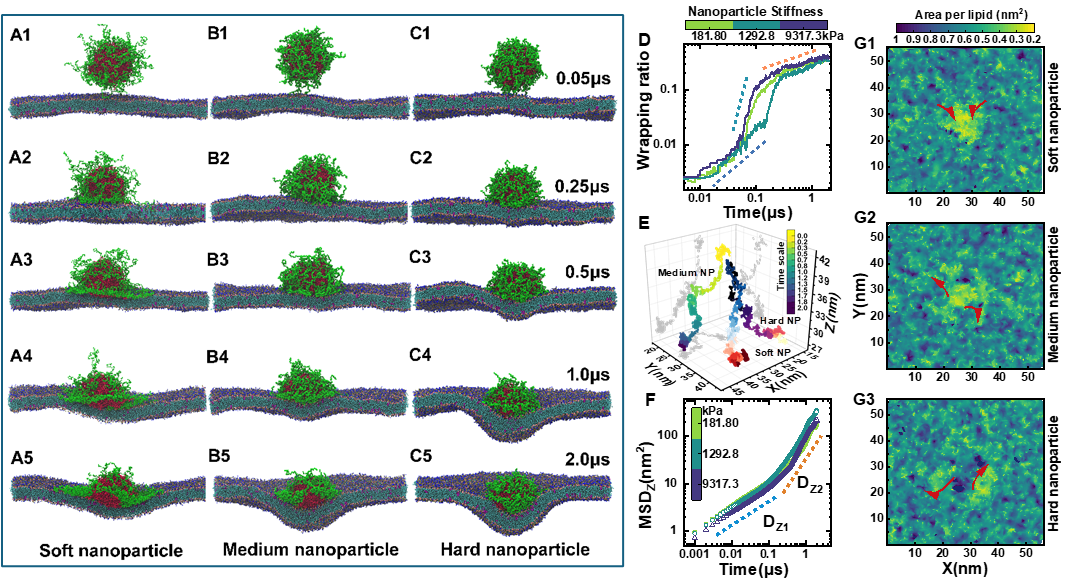
图2.不同弹性纳米颗粒(NPs)细胞穿透的内在动力学: (A-C)代表性快照, (D)膜包裹的典型时间序列记录, (E)弹性NP轨迹, (F)结构变形因子,以及(G1-G3)脂质膜的二维面积。快照颜色与图2A-2C相似。杨氏模量分别为68.9 kPa(软)、127.3 kPa(中)、5.2 MPa(硬),与后续研究中记录的数值一致。
图3展示了通过自由能分解揭示纳米颗粒(NP)刚度在膜穿透中的热力学调控机制:软NP的穿透由焓主导,在短程表现出强吸引力;硬NP的穿透则由熵主导,其刚性限制了焓贡献,却引起体系显著无序;中等刚度NP在二者间取得平衡,并随温度升高由焓驱动向熵驱动转变。该焓-熵竞争关系表明,NP刚度是决定其与膜相互作用热力学路径的关键物理参量。
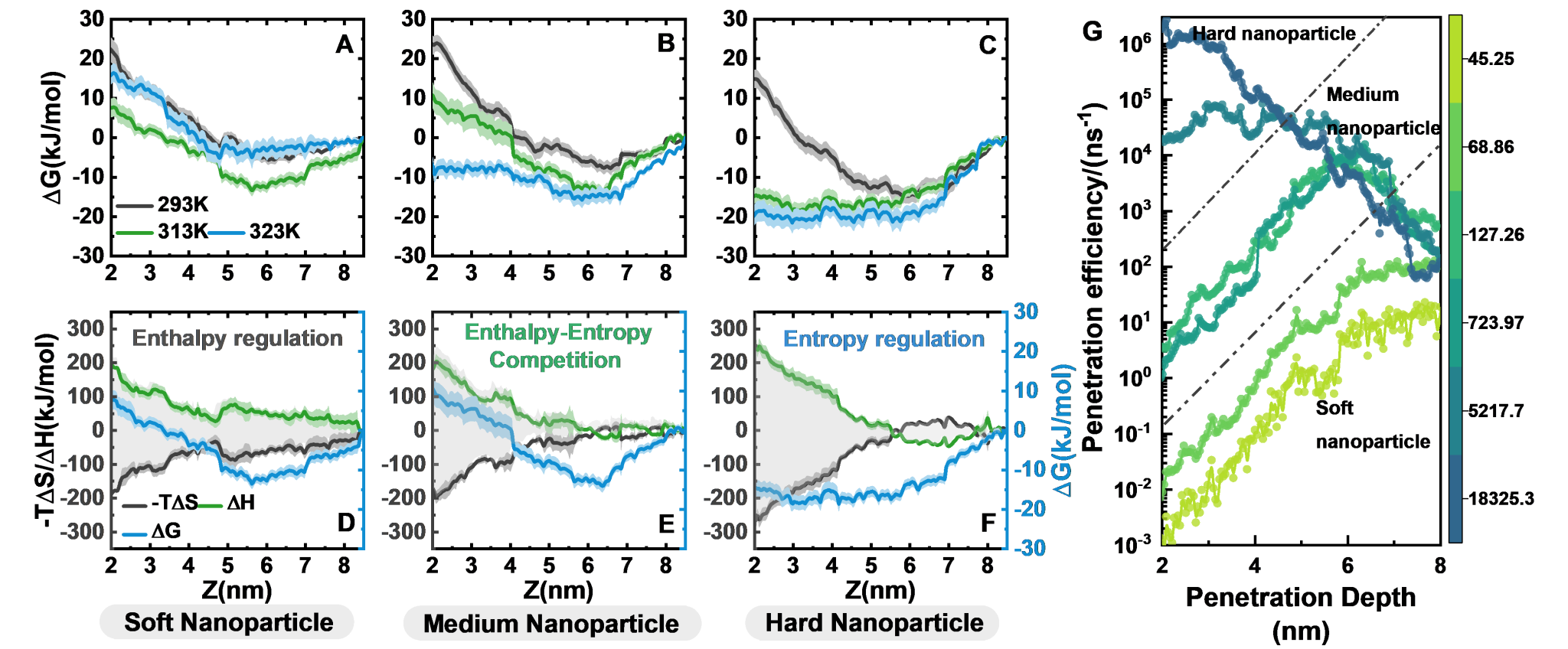
图3.弹性纳米颗粒生物膜穿透的变形焓-熵竞争证据:(A-C)弹性纳米颗粒穿透膜过程中随深度变化的吉布斯自由能ΔG,(E-F)熵贡献-TΔS,焓贡献ΔH,以及(G)随深度变化的穿透效率。
继而,课题组还建立了仿生膜囊泡模型(图4A),其脂质与受体比例为1:1,具有不对称弯曲结构。采用粗粒化方法将水分子简化为溶剂颗粒,脂质和受体采用H3(T5)2模型(图4B-C)。通过随机网络交联模型构建了均质、Janus型和核壳型聚合物纳米颗粒(图4D-F),其中亲水段(红色)和疏水段(青蓝色)分别表示,颗粒弹性通过交联度精确调控。该多尺度模型为研究纳米颗粒-膜相互作用提供了可靠基础。
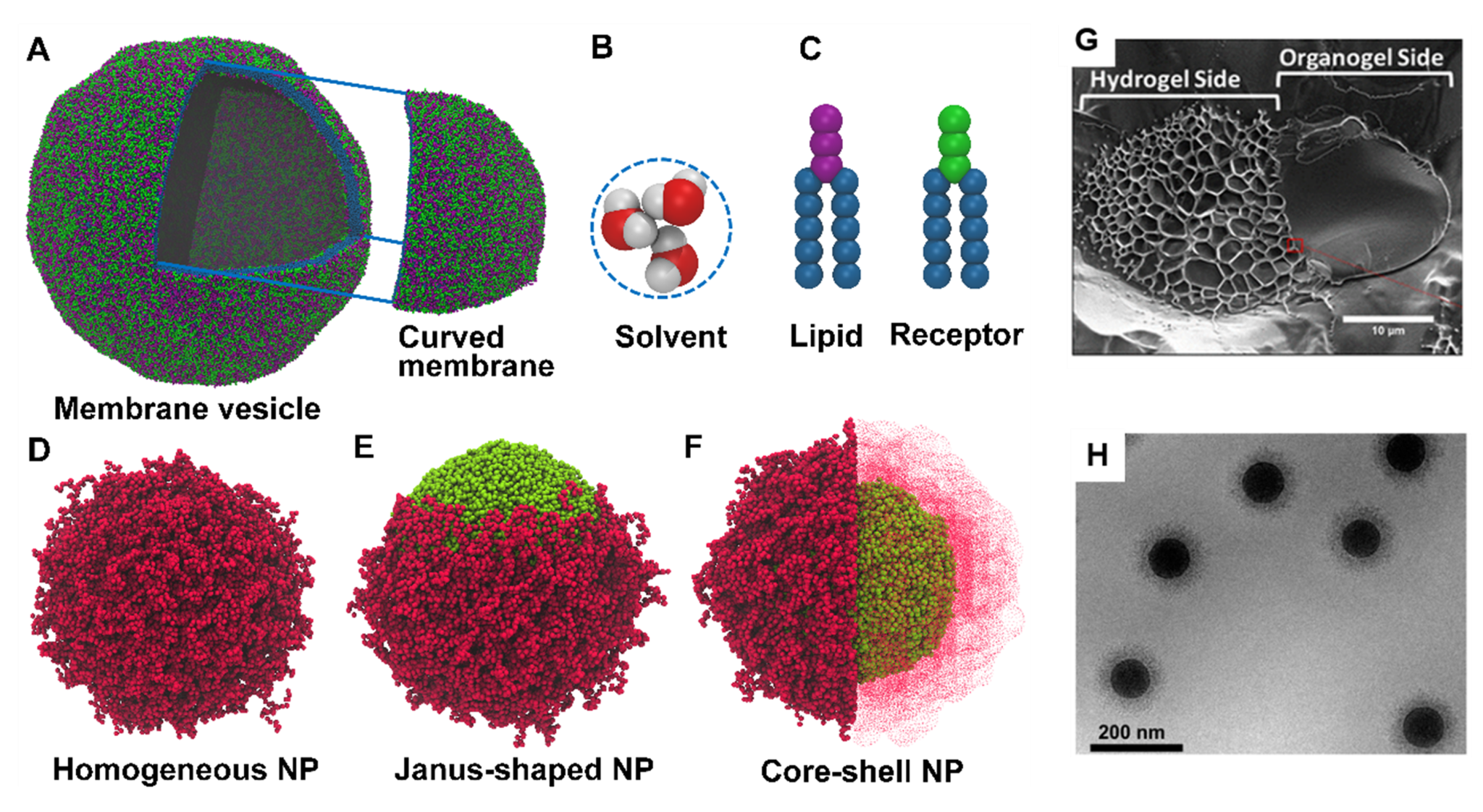
图4.粗粒度模型示意图,针对(A)膜囊泡,(B)溶剂,(C)脂质和受体,(D-F)具有多种结构的高分子NP,以及(G)核壳和(H)Janus非泡的冷冻扫描电镜图像。在聚合物NP模型中,亲水性PEG段用红色颗粒表示,而疏水段则用青蓝色颗粒表示。脂质和受体头由粉色和绿色颗粒表示,而脂质和受体尾部则由深蓝色颗粒表示。聚乙二醇二丙酸酯/聚丙二醇二丙烯酸酯Janus NP经参考文献许可复制。
图5通过系统比较三种纳米颗粒(NP)设计,揭示了结构异质性与网络弹性对细胞内化机制的协同调控。研究表明,均质NP在低刚度下通过"膨胀引导"的均匀变形促进膜破裂式内化,其松散网络结构(宽浅的S(q)散射峰)赋予高构型熵与膜适配性;而核壳NP因刚性核心的变形阻力主要引发膜包裹,其密集交联特征(高阶S(q)峰)限制了结构重构能力。低温透射电镜观测进一步验证了该机制:脂质在软质水凝胶中的均匀溶胀对应均质NP的膜破裂行为,而核壳NP的受限包裹则与脂质分散局限性一致。此发现阐明了纳米颗粒内部力学结构通过调控膜相互作用模式决定内化路径的物理本质。

图5.结构异质性与网络弹性在可变形聚合物NP细胞内化中的关系:(A)在不同机械强度和内部结构构型下内化路径和易位效率的示意图;(B)内化模式的代表性快照;(C)NP的静态结构因子;以及(D)实验性透射镜图像,显示嵌入水凝胶中的脂质纳米囊泡。易位效率由平衡态下的包裹比决定。(D)中的透射电子元件图像经Yu等人许可改编。
本研究由国家自然科学基金(项目编号:22478045和22178072)、重庆市自然科学基金(项目编号:CSTB2024NSCQ-QCXMX0099和CSTB2025NSCQ-LZX0099)以及重庆市教委科技研究项目(项目编号:KJZD-K202301202)资助。
文章相关链接:https://pubs.acs.org/doi/10.1021/acs.biomac.5c02216; https://doi.org/10.1016/j.colsurfb.2025.115302